原研药与仿制药区别:索托拉西布
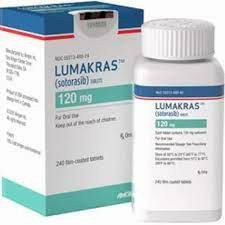
索托拉西布(AMG510,Sotorasib)是目前已被美国FDA和欧洲EMA批准上市的首个KRAS G12C突变特异性抑制剂,其作为原研药由安进(Amgen)公司开发并率先商业化,标志着KRAS“不可成药”时代的突破,用于治疗非小细胞肺癌(NSCLC)和结直肠癌。然而,关于索托拉西布的原研药与仿制药之间的差别,在全球用药市场引发了广泛关注。原研药,即由最初研发公司生产、拥有完整知识产权和临床数据支持的版本,具有高标准的工艺控制和一致性验证。以索托拉西布为例,其原研规格为120mg/片,每瓶包含240片,在国际市场(如美国或新加坡)销售价格高达人民币8万元左右。而在欧洲市场,价格有所下降,约在4万多元人民币。
与此同时,仿制药作为非原始研发但在成分、剂量和药理作用上高度相似的版本,逐渐成为部分患者的经济替代选择。在海外一些国家如老挝、印度等,由当地药厂如卢修斯(Lucius)生产的仿制版索托拉西布也已上市。例如,120mg*56片装的价格约为一千多元人民币,价格差距显著。虽然这类仿制药在结构和主成分上几乎一致,但由于未在中国或欧美取得正式上市许可,缺乏严格的临床等效性验证,使用时存在潜在风险。
从疗效层面而言,原研药通常伴随完整的临床路径、安全性评估、稳定性研究,且生产标准符合欧美法规。而仿制药则可能在原料药来源、制剂工艺及生物利用度方面存在微小差异,部分患者可能面临疗效不及预期或副作用波动的问题。因此,在选择索托拉西布时,若经济条件允许,原研药无疑是更具安全保障的选择;但对于部分资金有限的患者,合规渠道获得质量过关的仿制药也为维持治疗提供了现实选择。
参考资料:https://www.lumakras.com/
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。



















