Rytelo(Imetelstat)的说明书
一、名称:Rytelo(Imetelstat)
二、适应症:
Rytelo(Imetelstat)适用于治疗患有低至中度风险骨髓增生异常综合征(MDS)的成人患者,这些患者患有输血依赖性贫血,需要4个或更多红细胞单位超过8周,且对红细胞生成刺激剂(ESA)无反应或无反应或不合格。
三、用法用量:
1、推荐剂量:Rytelo的推荐剂量为7.1mg/kg,每4周静脉输注2小时。如果患者在接受24周治疗(注射6剂)后,红细胞(RBC)输血量没有减少,或者在任何时候出现不可接受的毒性,则应停用RYTELO。
2、推荐的术前用药:给药前至少30分钟患者可能需服用以下治疗前药物,以防止或减少潜在的输注相关反应:苯海拉明(或等效物)25mg至50mg,静脉注射或口服;氢化可的松(或等效物)100mg至200mg,静脉注射或口服;输液完成后,至少监测患者一小时的不良反应。
3、剂量调整:患者使用Rytelo后可能会出现不可耐受的不良反应,医生会根据病情的严重程度暂时延迟剂量、减少剂量或停止治疗,首次剂量可减少至每4周使用一次 5.6mg/kg;第二次剂量可减少至每4周使用一次4.4mg/kg;如果患者不能耐受4.4mg/kg的最低剂量水平,则应永久停止使用Rytelo治疗。
四、不良反应:
在Rytelo的临床研究中,最常见的不良反应(≥10%)为疲劳、关节痛/肌痛、新冠肺炎感染和头痛;实验室异常包括血小板减少、白细胞减少、中性粒细胞减少、天冬氨酸转氨酶(AST)增加、碱性磷酸酶增加、丙氨酸转氨酶(ALT)增加、部分凝血活酶时间延长。
五、供应和储存:
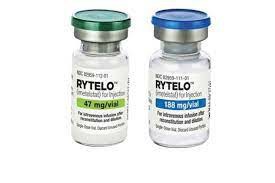
1、注射用Rytelo是一种不含防腐剂的白色至灰白色或微黄色冻干粉,可提供47mg单剂量小瓶、188mg单剂量小瓶,将小瓶冷藏在2°C至8°C(36°F至46°F)的原纸箱中。不要冻结。
2、稀释后的Rytelo溶液如果不立即使用,在室温20°C至25°C(68°F至77°F)下储存时;从复溶Rytelo到完成静脉输注的总时间不得超过18小时;冷藏储存时,温度为2°C至8°C(36°F至46°F),也不应超过复溶后的48小时。
六、特殊人群:
根据对动物的研究结果,Rytelo可能会损害具有生殖潜力的雌性动物的生育能力,对生育能力的影响是可逆的。因此建议具有生殖潜力的女性在使用Rytelo治疗期间以及最后一次给药后1周内使用有效的避孕措施;哺乳期妇女在使用Rytelo治疗期间以及最后一次给药后1周内不要进行母乳喂养。
七、作用机制:
Rytelo中的成分Imetelstat是一种寡核苷酸人端粒酶抑制剂,它结合到人端粒酶(hTR)RNA成分的模板区域,抑制端粒酶酶活性并阻止端粒结合。据报道,在骨髓增生异常综合征和恶性干细胞和祖细胞中,端粒酶活性和人端粒酶逆转录酶(hTERT)RNA表达增加。非临床研究表明,Imetelstat治疗导致端粒长度减少,恶性干细胞和祖细胞增殖减少,并诱导凋亡细胞死亡。
八、非临床毒理学
尚未使用Imetelstat进行致癌性研究。在体外,Imetelstat在细菌诱变性试验(Ames试验)中无诱变性,在使用培养的人外周血淋巴细胞进行的染色体畸变试验中无致染色体断裂性。在体内小鼠微核试验中,静脉注射剂量达到约104mg/kg时,Imetelstat没有遗传毒性。尚未使用Imetelstat进行生育力研究。在一项一般毒理学研究中,连续9个月每周一次服用14.1mg/kg的雌性猴子表现出子宫内膜萎缩。在推荐临床剂量下,平均暴露量(基于AUC)约为人类暴露量的14.4倍时观察到这种影响。这一发现在14周恢复期后的动物中没有出现。
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。



















