FDA加速批准AVMAPKI聯合FAKZYNJA治療KRAS突變復發性低級別漿液性卵巢癌的最新進展
2025年5月9日,生物製藥公司Verastem Oncology宣布,美國食品藥品監督管理局(FDA)已加速批准其聯合用藥AVMAPKI(avutometinib膠囊)和FAKZYNJA(defactinib片劑),用於治療先前接受過全身治療且具有KRAS基因突變的複發性低級別漿液性卵巢癌(LGSOC)成年患者。這一批准標誌著LGSOC患者的治療領域邁出了重要一步,為這部分患者提供了新的治療選擇。
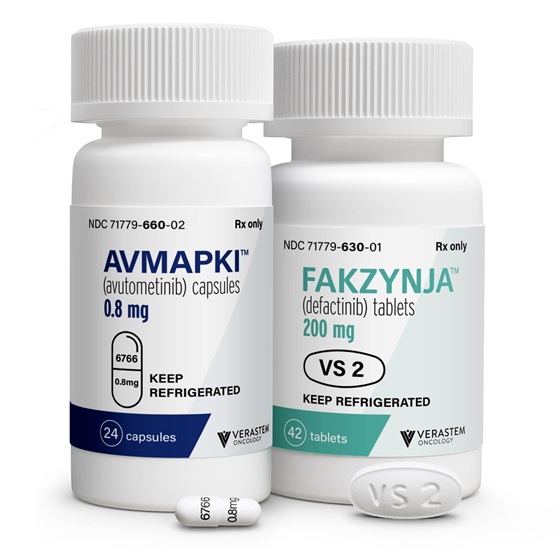
AVMAPKI和FAKZYNJA均由Verastem Oncology研發,AVMAPKI膠囊規格為0.8毫克,FAKZYNJA片劑規格為200毫克。 AVMAPKI為白色膠囊,膠囊蓋印有“6766”,膠囊體印有“0.8mg”,FAKZYNJA則為橢圓形白至灰白色片劑,單面有“VS2”的凹陷標記。兩種藥物需在2℃至8℃冰箱中保存,確保藥效穩定。
這套聯合用藥的適應症為治療曾接受全身治療且腫瘤中存在KRAS突變的複發性LGSOC患者。用法用量方面,AVMAPKI在每個28天週期的前3週內,每周口服兩次,每次劑量為3.2毫克(4粒0.8毫克膠囊),建議隨餐服用且整粒吞服。 FAKZYNJA則為每日兩次,每次200毫克,亦隨餐服用,藥片須整片服用不可咀嚼或破碎。
在患者篩選過程中,需通過腫瘤標本檢測確認KRAS突變陽性,以確保治療的針對性。目前FDA尚未批准用於LGSOC KRAS突變檢測的官方試驗,但這一分子標誌物是選擇該聯合治療的關鍵依據。此外,治療期間需注意眼部健康,每隔數週期進行全面眼科檢查,預防及早發現潛在的眼毒性問題。同時,聯合用藥的皮膚毒性較為常見,因此建議使用局部類固醇和全身口服抗生素作為預防措施。
不良反應方面,患者最常見的副作用包括肌酸磷酸激酶升高、噁心、疲勞、皮疹、腹瀉及肝功能異常等。此外,眼部毒性如玻璃體視網膜病變、視力障礙需密切監控,若症狀出現或加重,應及時調整用藥。肝功能和肌酸磷酸激酶水平的監測同樣重要,以避免嚴重毒性反應。孕婦及育齡期女性應避免用藥,且治療期間及停藥後需採取有效避孕措施,避免胎兒風險。
在藥物相互作用方面,FAKZYNJA為CYP3A4代謝底物,使用時需避免與強效CYP3A4抑製劑或誘導劑合用,以免影響藥效或增加毒性風險。此外,患者若需同時服用華法林,需密切監測凝血功能。胃酸減少劑如質子泵抑製劑可能降低FAKZYNJA吸收,使用時應調整給藥時間,確保療效。
特別人群使用方面,尚無明確的兒科用藥數據,老年患者反應尚不完全明確。哺乳期婦女應避免用藥期間及停藥後2週內母乳喂養,以防兒童發生嚴重不良反應。該聯合治療還可能對男性和女性生育能力產生不良影響,需提前告知患者相關風險。
患者使用該藥時應嚴格遵照醫囑,定期進行眼科和實驗室檢查,及時報告任何異常症狀。治療期間應注意防曬,減少光敏反應的發生,若出現嚴重皮膚或眼部症狀,應盡快就醫。通過科學合理的用藥管理和密切監護,AVMAPKI聯合FAKZYNJA為KRAS突變復發性LGSOC患者帶來了新的治療希望。
總結而言,FDA對AVMAPKI與FAKZYNJA的加速批准,為KRAS突變復發性低級別漿液性卵巢癌患者提供了有效的治療新方案。患者和臨床醫生應密切配合,合理應用該藥物組合,最大化其治療效果並有效控制副作用,助力患者戰勝疾病。
參考資料:
https://www.verastem.com/pdf/avmapki-fakzynja-co-pack-full-prescribing-information.pdf
[ 免责声明 ] 本页面内容来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供持有医疗专业资质的人员用于医学药学研究参考,不构成任何治疗建议或药品推荐。所涉药品可能未在中国大陆获批上市,不适用于中国境内销售和使用。如需治疗,请咨询正规医疗机构。本站不提供药品销售或代购服务。
.jpeg)


















